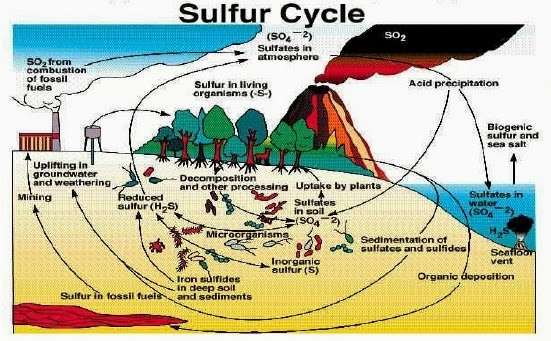
Siklus belerang/sulfur adalah perubahan sulfur dari hidrogen sulfida menjadi sulfur dioksida lalu menjadi sulfat dan kembali menjadi hidrogen sulfida lagi.
Bagaimana siklus sulfur atau belerang di dalam tanah ?
Siklus belerang/sulfur adalah perubahan sulfur dari hidrogen sulfida menjadi sulfur dioksida lalu menjadi sulfat dan kembali menjadi hidrogen sulfida lagi.
Bagaimana siklus sulfur atau belerang di dalam tanah ?

Total S dalam tanah bervariasi mulai dari sangat sedikit sampai dengan 1000 mg S per kg tanah (0.1%), nilai yang lebih tinggi dapat ditemui pada tanah-tanah bermasalah seperti tanah salin dan tanah sulfat masam (Takkar, 1988; Genesmurthy et. al., 1989). Sulfur dalam tanah terdapat dalam bentuk organik dan anorganik.
Bentuk S anorganik penting ada dalam tanah sebab sebagian besar sulfur diambil oleh tanaman dalam bentuk SO42- (sulfat), begitu juga bentuk S organik juga penting ada dalam tanah karena dapat meningkatkan total S tanah (Prasad dan Power, 1997). Sebagian besar bentuk sulfur di dalam tanah adalah S organik (Stevenson, 1982). Hampir semua sulfur dalam tanah tropis yang tidak dipupuk terdapat dalam bentuk organik. Kadar S dalam tanah bervariasi dan dipengaruhi oleh penambahan sulfur dari bahan organik, air irigasi, udara, pupuk dan pestisida.
Sulfur diserap oleh tanaman dalam bentuk sulfat (SO42-) dan hanya sebagian kecil sulfur dalam bentuk gas SO2 yang diserap langsung oleh tanaman dari tanah dan atmosfer. Bentuk S tersebut merupakan S anorganik yang bersifat aktif di dalam tanah. Sulfur anorganik dihasilkan dari dekomposisi senyawa organik yang mengandung S dan dari pupuk pembawa S (Engelstad, 1997). Bentuk sulfur anorganik yaitu SO42- terlarut, SO42- terjerap, SO42- tak larut dan S anorganik tereduksi. SO42- terlarut dan terjerap merupakan fraksi sulfur
yang dapat tersedia bagi tanaman (Tisdale et.al, 1985).
Kandungan sulfat terlarut dalam tanah menurut Prasad dan Power (1997) bervarasi tergantung dari beberapa faktor yaitu :
Di daerah tropika basah seperti Indonesia sulfat mudah hilang dari tanah melalui berbagai cara, yaitu terangkut oleh tanaman dan organisme tanah, tererosi, dan tercuci. Pengelolaan tanah dan tanaman menentukan keberadaan sulfat karena erosi. Tekstur yang kasar mempercepat kehilangan sulfat.
Pencucian sulfat dari lapisan bagian atas tanah dapat merupakan penyebab terjadinya kekurangan S dibagian tersebut. Jerapan sulfat dipengaruhi oleh sejumlah sifat tanah, antara lain: jumlah (kadar) dan tipe mineral liat, hidroksida, horison atau ke dalaman tanah, pH, konsentrasi sulfat, waktu kehadiran anion lain dan bahan organik (Tisdale et al. 1985).
Nisbah C:N:S dalam bahan organik adalah sekitar 125 : 10 : 1.2. Dalam keadaan aerobik bakteri yang sama dapat mengoksidasi S menjadi H2S04. Unsur S dapat pula dioksidasi oleh bakteri Khemotropik dari genus Tiobacillus (Mengel dan Kirkby, 1987).
Ketersediaan S dalam tanah tergantung pada beberapa faktor terutama redoks potensial tanah, kandungan bahan organik, aktivitas mikroorgnisme tanah, kualitas air pengairan dan air hujan (Blair et.al., 1977). Penambahan sulfur baik yang berasal dari bahan organik maupun anorganik pada beberapa sistem pertanian dapat meningkatkan bahan organik, total sulfur organik, dan mineralisasi S. Tanaman mendapatkan sulfat tersedia selain dari tanah dan pupuk yang membawa S juga mendapatkan sulfur dari air pengairan, air hujan, dan udara. Oleh karena itu untuk menduga kebutuhan sulfur tanaman dalam rangka penentuan dosis pupuk tidak cukup hanya berdasarkan pengamatan S tanah.
Dalam keadaan anaerob seperti pada lahan sawah yang tergenang terjadi reduksi sulfat menjadi sulfida.
Menurut Anwar (2000), bahwa sulfat bertendensi tidak mantap dalam lingkungan anaerobik. Reduksi sulfat menjadi sulfida (H2S) oleh bakteri Desulvovibrio desulfuricans, yang selanjutnya bereaksi dengan ion Fe2+ dalam larutan dan membentuk ferro sulfida (FeS) atau “macknawite”, kemudian bereaksi dengan sulfur (S) dan menghasilkan FeS2 (ferro disulfida) dengan reaksi sebagai berikut :
Fe(OH)2 + H2S → FeS + 2 H2O
FeS + S +e → FeS2
Reaksi tersebut berkaitan dengan oksidasi bahan organik (elektron donor atau proton donor) atau respirasi yang memerlukan alternatif elektron akseptor (Oksigen, Nitrat, Oksida mangan, besi, sulfat yang akan direduksi). Reaksi tersebut akan mengakibatkan berkurangnya sulfat tersedia bagi tanaman di dalam tanah.
Sulfat dalam tanah aerob dapat tereduksi oleh bakteri membentuk H2S yang pada gilirannya akan bereaksi dengan logam-logam berat menghasilkan sulfida-sulfida yang sangat tidak larut. Selain itu, tingginya kandungan Ca2+ pada tanah dapat mengurangi kelarutan SO42- (Engelstad, 1997). Oleh karena itu pada tanah-tanah alkalin dan tanah yang dikapur berlebihan tanaman sering mengalami kekurangan sulfur.
Senyawa organik yang dilepaskan eksudat akar dan mikroba memegang peranan penting dalam menentukan ketersediaan ion sulfat dalam tanah. Kimura et.al. (1991) menyatakan bahwa ion sulfat dalam tanah akan direduksi oleh H2 yang berasal dari eksudat dan H2 yang dilepaskan oleh bahan organik. Sejumlah sulfur ditemukan pada horizon permukaan dalam bentuk S organik. Secara umum S organik pada top soil permukaan lebih tinggi dari pada subsoil.
Secara umum jumlah S yang termineralisasi dari tanah secara tidak langsung berhubungan dengan tipe tanah, C, N atau S, C:N, N:S, C:S rasio, pH tanah, atau N yang termineralisasi. Rasio C:S menunjukkan ukuran kemudahan bahan organik melepaskan sulfat ke dalam tanah. Freney (1986) mengemukakan bahwa SO42+ dilepaskan dari bahan organik pada saat C:S rasio dibawah 200 dan diimobilisasi saat rasio lebih besar dari 400. Immobilisasi dan mineralisasi terjadi keduanya pada saat rasio antara 200 dan 400. Oleh
karena itu, pupuk organik yang akan diberikan harus telah dikomposkan terlebih dahulu sehingga nilai rasio C:S nya dibawah 200.
Siklus S (belerang) dalam tanah mencerminkan ketersediaan belerang dalam tanah dengan melibatkan proses penambahan, pengurangan, dan keseimbangan S dalam larutan tanah.
Bentuk S yang langsung diserap tanaman adalah SO42- dan sedikit dalam bentuk SO2 (gas).
Belerang sangat penting dalam penyusun jaringan tanaman seperti penyusun utama protein (asam amino metionin, sistein, dan sistin), dan penyusun vitamin (biotin dan tiamin) dan khlorofil. Kebutuhan tanaman akan S hampir sama dengan P sebagai unsur hara esensial makro (Nyakpa dkk 1988).
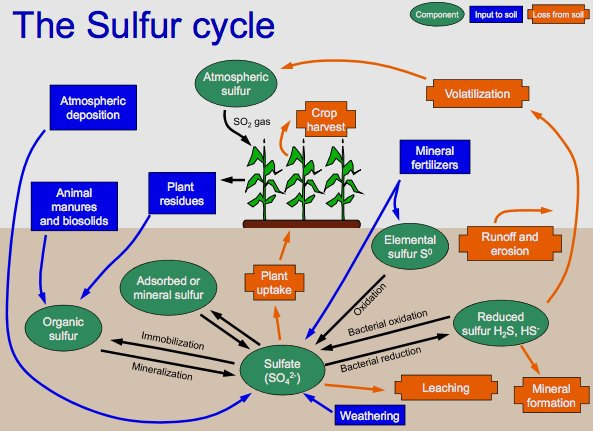
Gambar Siklus Belerang (S) dalam tanah
Siklus S dalam tanah dapat dijelaskan sebagai berikut:
Perubahan unsur S ke SO42- atau H2S bergantung pada kondisi tanah anaerob atau aerob.
Bila tanah anaerob, akan dihasilkan H2S (gas), bila tanah aerob, akan dihasilkan SO42-. Sulfat, SO42- sangat mudah tercuci dan hilang dari profil tanah, tetapi sebagian diserap tanaman dan diubah menjadi S organik dalam jaringan tanaman. Bila tanaman mati, S organik akan didekomposisi menjadi S anorganik di dalam tanah.
Bila tanah aerob, S anorganik akan berubah menjadi SO42-, dan bila tanah anaerob, SO42- berubah menjadi H2S (gas). Hidrogen Sulfida, H2S dapat hilang ke atmosfir atau berubah menjadi S anorganik dengan bantuan bakteri fotosintetik dan bakteri khemotropik. Bila ada besi (Fe) di dalam tanah, H2S akan diubah menjadi FeS2, yang dikenal dengan mineral Pirit (Mengel & Kirby 1987).