Nitrogen memiliki banyak bentuk kimia, baik organik maupun anorganik.
Nitrogen organik berasosiasi dengan karbon, sedangkan nitrogen anorganik berasosiasi dengan elemen lain selain karbon. Beberapa nitrogen anorganik diantaranya, yaitu nitrat (NO3-), nitrit (NO2-), amonium (NH4+), dan amonia (NH3) (Barsanti & Gualtieri 2006).
Nitrogen dapat ditemukan dalam 4 lapisan berbeda di bumi, yaitu atmosfer, biosfer, hidrosfer, dan litosfer. Lapisan atmosfer mengandung ± 80% nitrogen (N2) (Hubbell & Kidder 2003). Nitrogen (N2) bebas di udara memiliki ikatan rangkap 3, sehingga molekul tersebut bersifat sangat stabil. Hanya sejumlah kecil (5–8%) nitrogen yang dapat ditambat secara alami oleh alam melalui temperatur dan tekanan tinggi saat terjadi petir (Barsanti & Gualtieri 2006).
Pertumbuhan organisme bergantung pada ketersediaan nutrien. Nitrogen merupakan salah satu nutrien penting yang dibutuhkan dalam jumlah besar sebagai penyusun dari peptida, protein enzim, klorofil, molekul transfer-energi (ATP, ADP), dan materi genetik (RNA, DNA) (Barsanti & Gualtieri 2006). Nitrogen harus direduksi terlebih dahulu menjadi amonia agar dapat digunakan oleh organisme dalam proses metabolisme (Frank dkk. 2003).
Fiksasi nitrogen merupakan suatu proses reduksi dinitrogen (N2) menjadi amonia (NH3) yang dikatalis oleh enzim nitrogenase. Fiksasi nitrogen hanya dapat dilakukan oleh organisme prokariot, karena enzim nitrogenase hanya dikode pada genome prokariot (Fay 1992). Fiksasi nitrogen pada Nostoc terjadi pada sel khusus yang disebut heterokis (Kumar 1985).
Reaksi fiksasi nitrogen [Barney dkk. 2007] adalah sebagai berikut :
N2 + 8 H+ + 8e- + 16 MgATP 2 NH3 + H2 + 16 MgADP + 16 Pi
Amonia (NH3) hasil fiksasi nitrogen akan bergabung dengan 2-oxoglutarat (hasil siklus Asam sitrat) dan membentuk glutamat. Proses perubahan tersebut dilakukan dengan bantuan enzim glutamate dehidrogenase. Penambahan amonium kedua pada glutamat akan menghasilkan glutamin. Molekul glutamin inilah yang kemudian ditransfer dari sel heterokis ke sel vegetatif yang berada di sebelah sel heterokis (Sah 2008).
Cyanobacteria adalah mikroorganisme prokariot yang memperoleh energi melalui proses fotosintesis. Reaksi fotosintesis pada Cyanobacteria terjadi melalui fotosistem yang sama seperti pada tumbuhan tingkat tinggi.
Cyanobacteria merupakan satu-satunya mikroorganisme yang mampu melakukan fotosintesis (yang melibatkan oksigen) sekaligus fiksasi nitrogen (Thiel 2004).
Fotosintesis meliputi proses yang terjadi pada 2 fotosistem berbeda, yaitu fotosistem I dan fotosistem II. Kedua fotosistem tersebut terhubung dalam suatu untaian dan berinteraksi melalui rantai transpor elektron (Fay 1992).
Sebagian besar Cyanobacteria memiliki kemampuan untuk melakukan fotosintesis pada kondisi aerob maupun anaerob. Ketika kondisi aerob, elektron yang dibutuhkan fotosistem I berasal dari fotosistem II. Ketika kondisi anaerob dengan keberadaan sulfur, maka elektron didapat dari reduksi sulfur (Lee 2008).
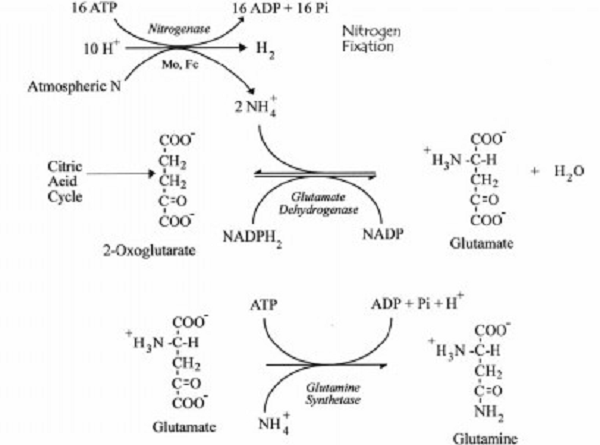
Gambar Reaksi Kimia Perubahan Molekul Amonium menjadi Glutamin [Sumber: Lee 2008.]
Reaksi fotosintesis pada sebagian besar Cyanobacteria terinduksi oleh konsentrasi oksigen yang rendah. Fenomena tersebut menggambarkan adaptasi Cyanobacteria terhadap ketiadaan oksigen di atmosfer pada era Precambrian (Lee 2008). Cyanobacteria diduga merupakan organisme fotosintetik pertama yang melibatkan oksigen dan berperan dalam mengubah atmosfer bumi dari keadaaan tanpa oksigen menjadi kondisi atmosfer yang sekarang (Boonkerd dkk. 2002).
Beberapa penelitian menunjukkan bahwa mungkin terdapat hubungan antara frekuensi sel heterokis dengan aktivitas enzim nitrogenase pada strain Cyanobacteria aerob (Stewart 1980). Meskipun demikian, hubungan yang terbentuk sangat bervariasi tergantung pada keadaan metabolisme strain (Stewart 1980).
Penelitian Moghadam & Nowruzi (2008) pada strain Nostoc ellipsosporum dan Nostoc muscorum menunjukkan bahwa mungkin terdapat hubungan antara ukuran sel heterokis dengan laju fiksasi nitrogen. Hasil penelitian menunjukkan bahwa N. ellipsosporum memiliki ukuran sel heterokis yang lebih besar dan laju fiksasi nitrogen yang lebih tinggi dibandingkan N. muscorum.
Meskipun demikian, perlu dilakukan penelitian lanjutan untuk memastikan bahwa memang terdapat hubungan antara ukuran sel heterokis dalam filamen dengan laju fiksasi nitrogen (Moghadam & Nowruzi 2008).
Fiksasi nitrogen bergantung pada fotosintesis dalam menyediakan ATP sebagai sumber energi dan komponen karbon sebagai donor elektron. Durasi dan laju fiksasi nitrogen bergantung pada kondisi yang memengaruhi keseimbangan karbon, seperti kelembapan, suhu, dan intensitas cahaya. Sel Nostoc aktif secara fisiologis hanya dalam keadaan lembap. Tingkat kelembapan yang diperlukan sel Nostoc dalam proses inisiasi dan optimalisasi fiksasi nitrogen bervariasi untuk setiap spesies dan habitat. Sebagian besar Cyanobacteria dapat melakukan fiksasi nitrogen pada suhu antara (-5)–30° C. Suhu optimum fiksasi nitrogen pada Nostoc adalah 28° C, sedangkan suhu minimum berkisar antara (-7,6)–0° C pada Nostoc yang hidup bebas maupun berasosiasi dengan lichen (Belnap 2001)
Fiksasi nitrogen dikatalis oleh enzim nitrogenase yang terdapat di dalam sel heterokis. Enzim nitrogenase adalah kompleks enzim yang berfungsi mengkatalis reduksi dinitrogen bebas di udara menjadi amonia dalam proses fiksasi nitrogen (Barney dkk . 2007). Enzim nitrogenase mampu mengikat dan mereduksi substrat lain selain dinitrogen (N2) bebas di udara, diantaranya asetilen (C2H2) (Hellebust & Craigie 1978).
Enzim nitrogenase sangat sensitif terhadap oksigen. Enzim nitrogenase akan dengan cepat mengalami inaktivasi yang bersifat permanen ketika terpapar oleh oksigen. Penelitian terhadap semua mikroorganisme penambat nitrogen menunjukkan terdapat kesamaan karakteristik biokimia dan sifat sensitif enzim nitrogenase terhadap oksigen (Fay 1992).
Nostoc tidak membentuk sel heterokis maupun enzim nitrogenase apabila ditumbuhkan pada medium dengan kandungan nitrogen (Stewart 1980).
Keberadaan sumber nitrogen, seperti amonium atau nitrat, akan menghambat diferensiasi sel heterokis (Kumar dkk. 2010). Penelitian Kumar dkk. (2010) pada Anabaena PCC 7120 yang ditumbuhkan pada medium yang mengandung amonium atau nitrat menunjukkan bahwa spesies tersebut tumbuh membentuk filamen panjang berupa ratusan sel vegetatif tanpa adanya sel heterokis. Apabila Anabaena ditumbuhkan pada medium tanpa nitrogen, akan terbentuk satu sel heterokis pada setiap 10–20 sel vegetatif sepanjang filamen.
Struktur enzim nitrogenase pada Nostoc sama dengan struktur enzim nitrogenase pada bakteri. Enzim nitrogenase tersusun atas 2 komponen, yaitu dinitrogenase reductase (protein besi) dan dinitrogenase (protein molybdenum- besi) yang dikode oleh operon nif HDK (Lee 2008).
-
Dinitrogenase reductase berbentuk dimer tersusun atas 2 subunit identik dengan gugus (4Fe-4S) tunggal dan memiliki berat molekul sebesar 64 kDa.
-
Dinitrogenase berbentuk tetramer dengan 2 pasang subunit yang berbeda, terdiri dari 4 gugus (4Fe-4S) dan 2 molekul kofaktor Mo-Fe (Frank dkk . 2003).
Mo-Fe kofaktor merupakan komponen penting dari dinitrogenase, tersusun atas 8 atom Fe dan 6 atom S per atom Mo. Berat molekul dari dinitrogenase adalah sebesar 245 kDa (Bohme, 1998).

