Katalase merupakan bagian dari sistem pertahanan enzimatik terhadap radikal bebas. Enzim ini mengkatalisis konversi hidrogen peroksida menjadi molekul air dan oksigen. Katalase terutama terdapat dalam peroksisom, dan sedikit di dalam fraksi sitosol dan mikrosom sel. Pada hati tikus, katalase juga terdapat di dalam mitokondria. Peroksisom juga kaya akan oksidase yang menghasilkan H2O2; organel ini merupakan salah satu bentuk mekanisme pertahanan kompartemensi terhadap radikal bebas.
Apa yang dimaksud dengan enzim Katalase?
Katalase (nomor klasifikasi enzim EC 1.15.1.6) merupakan enzim yang mengkatalisis konversi hidrogen peroksida (H2O2) menjadi molekul air dan oksigen. Di samping memiliki aktivitas peroksidase, enzim ini mamu menggunakan 1 molekul H2O2 sebagai substrat atau donor elektron dan molekul H2O2 yang lain sebagai oksidan atau akseptor elektron.
2H2O2 à 2H2O + O2
Enzim ini diproduksi oleh organisme aerobik, mulai organisme uniseluler seperti bakteri hingga manusia.30 Gen yang memproduksi katalase pada manusia telah diidentifikasi. Gen tersebut memiliki basa sepanjang 34 kb dan terpisah menjadi 13 ekson.
Katalase terutama terdapat dalam peroksisom, dan sedikit di dalam fraksi sitosol dan mikrosom sel.24-30,44 Pada sebuah penelitian, didapatkan bahwa pada hati tikus, katalase juga terdapat di dalam mitokondria.45 Peroksisom kaya akan oksidase dan katalase, yang merupakan salah satu bentuk mekanisme pertahanan kompartemensi terhadap radikal bebas.
Struktur Katalase
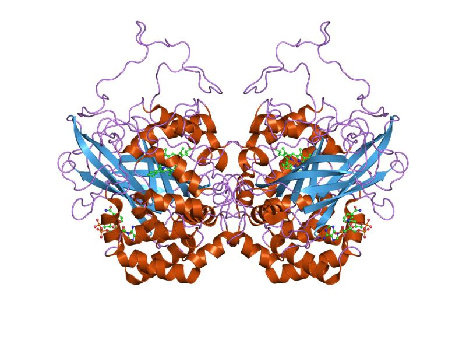
Katalase merupakan protein dengan struktur tetramer berbentuk dumbbell . Tetramernya terdiri dari subunit-subunit yang identik dengan berat molekul (BM) 220,000 sampai 350,000 kDa.46 Sebagian katalase terdapat dalam bentuk tetramer dengan berat molekul 60 atau 75 kDa. Setiap subunit (monomer) mengandung gugus heme (Fe3+) di pusat katalitiknya. Gugus heme ini terhubung keluar melalui saluran hidrofobik. Ion Fe3+ yang terdapat di molekul katalase berperan dalam katalisasi cepat pemecahan H2O2. Pemindahan ion Fe3+ dari subunit protein katalase mengakibatkan molekul protein kehilangan aktivitas katalitiknya.
Selain itu, monomer katalase dari spesies tertentu tiap subunit biasanya juga mengandung 1 molekul NADPH yang membantu menstabilkan enzim. NADP mungkin berperan sebagai kofaktor, mencegah pembentukan komponen inaktif dan melindungi enzim dari oksidasi oleh substratnya, hidrogen peroksida.46 Struktur katalase sangat rigid dan stabil, resisten terhadap unfolding , yang menyebabkan katalase bersifat stabil. Enzim ini lebih resisten terhadap pH, denaturasi termal, dan proteolisis dibanding enzim-enzim lain. Stabilitas dan resistensi terhadap proteolisis yang dimiliki katalase merupakan keuntungan evolusioner, terutama karena enzim ini diproduksi selama fase stasioner pertumbuhan sel di mana kadar protease tinggi dan laju turnover protein tinggi.
Mekanisme Kerja
Katalase mampu mengkatalasis reaksi penguraian hidrogen peroksida (H2O2) melalui 2 mekanisme kerja yaitu katalitik dan peroksidatik.
-
Mekanisme katalitik
Terjadi bila enzim ini menggunakan molekul H2O2 sebagai substrat atau donor elektron dan molekul H2O2 yang lain sebagai oksidan atau akseptor elektron. Proses katalitik diduga terjadi dalam 2 tahap di mana H2O2 mengoksidasi kemudian mereduksi besi heme pada tempat aktif enzim. Tahap I: molekul H2O2 mengoksidasi heme menjadi spesies oksiferri
Katalase-Fe (III) + H2O2 -> senyawa 1
Senyawa 1 + H2O2 -> katalase-Fe (III) + 2 H2O + O2
Tahap II: molekul H2O2 kedua digunakan sebagai reduktan untuk meregenerasi enzim, menghasilkan H2O dan O2.
-
Mekanisme peroksidatik
Terjadi bila menggunakan 1 molekul H2O2 sebagai akseptor elektron dan senyawa lain sebagai donor elektron. Senyawa yang dapat berperan sebagai donor elektron antara lain metanol, etanol, asam formiat, dan ion nitrit. Mekanisme ini dapat digambarkan sebagai berikut :
Katalase-Fe (III) + H2O2 -> senyawa 1
Senyawa 1 + AH2-> katalase-Fe (III) + 2 H2O + A
Senyawa donor elektron yang berupa metanol dan etanol akan dioksidasi menjadi aldehid yang sesuai yaitu formaldehid dan asetaldehid sedangkan asam formiat dioksidasi menjadi karbon dioksida dan ion nitrit dioksidasi menjadi nitrat.
Aktivitas katalase dapat dihambat oleh azida, sianida, dan asam hipoklorit (HOCL). Zat-zat ini selain dapat menghambat aktivitas katalase juga menghambat aktivitas banyak enzim lain. Inhibitor yang kuat untuk enzim katalase adalah aminotriazol. Aminotrizol menghambat aktivitas enzim katalase dengan cara mengikat senyawa 1 yang merupakan senyawa antara katalase-hidrogen peroksida.
Aktivitas katalase terutama ditemukan pada peroksisom sedangkan pada mitokondria, kloroplas dan retikulum endoplasma aktivitas katalase rendah. Enzim katalase dapat bekerja pada pH 4-8,5 namun aktivitas maksimum katalase diperoleh pada pH 7. Pada kisaran pH yang jauh dari pH optimum yaitu dibawah pH 4 atau diatas pH 8,5 terjadi inaktivasi enzim.
1 Like
