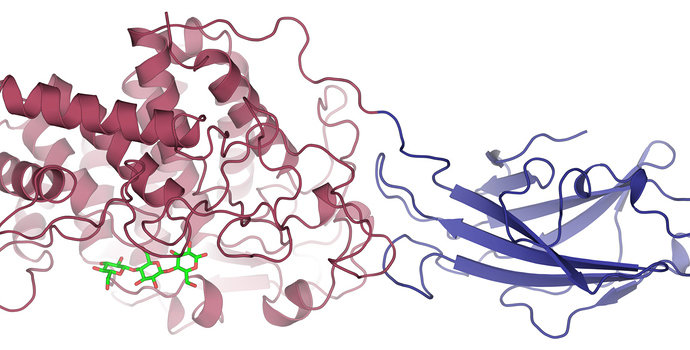
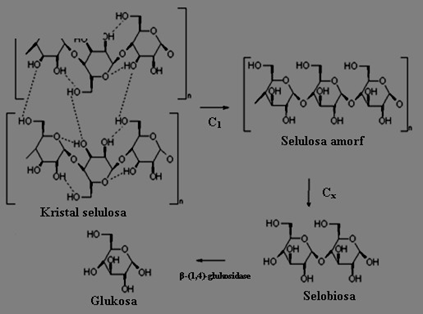
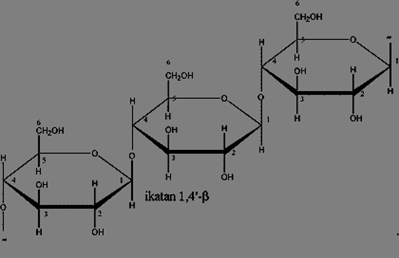
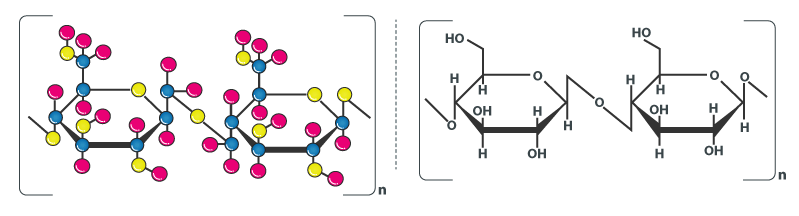
Selulosa (C6H10O5)n adalah polimer berantai panjang polisakarida karbonhidrat, dari beta-glukosa. Selulosa merupakan komponen utama dalam pembuatan kertas. Selulosa adalah senyawa organik penyusun utama dinding sel dari tumbuhan. Adapun sifat dari selulosa adalah berbentuk senyawa berserat, mempunyai tegangan tarik yang tinggi, tidak larut dalam air, dan pelarut organik.
Selulosa merupakan bagian utama susunan jaringan tanaman berkayu, bahan tersebut terdapat juga pada tumbuhan perdu seperti paku, lumut, ganggang dan jamur. Penggunaan terbesar selulosa yang berupa serat kayu dalam industri kertas dan produk turunan kertas lainnya.
Selulosa merupakan komponen penting dari kayu yang digunakan sebagai bahan baku pembuatan kertas.
Selulosa, oleh Casey (1960), didefinisikan sebagai karbohidrat yang dalam porsi besar mengandung lapisan dinding sebagian besar sel tumbuhan. Winarno (1997) menyebutkan bahwa selulosa merupakan serat-serat panjang yang bersama hemiselulosa, pektin, dan protein membentuk struktur jaringan yang memperkuat dinding sel tanaman. Macdonald dan Franklin (1969) menyebutkan bahwa selulosa adalah senyawa organik yang terdapat paling banyak di dunia dan merupakan bagian dari kayu dan tumbuhan tingkat tinggi lainnya. Fengel dan Wegener 1995 menyatakan bahwa selulosa terdapat pada semua tanaman dari pohon bertingkat tinggi hingga organisme primitif seperti rumput laut, flagelata, dan bakteri.
Selulosa merupakan polisakarida dengan rumus kimia (C6H10O5)n. Dalam hal ini adalah jumlah pengulangan unit gula atau derajat polimerisasi yang harganya bervariasi berdasarkan sumber selulosa dan perlakuan yang diterimanya. Kebanyakan serat untuk pembuatan pulp mempunyai harga derajat polimerisasi 600 – 1500.
Selulosa terdapat pada sebagian besar dinding sel dan bagian-bagian berkayu dari tumbuh-tumbuhan. Selulosa mempunyai peran yang menentukan karakter serat dan memungkinkan penggunaannya dalam pembuatan kertas. Dalam pembuatan pulp diharapkan serat-serat mempunyai kadar selulosa yang tinggi.
Sifat-sifat bahan yang mengandung selulosa berhubungan dengan derajat polimerisasi molekul selulosa. Berkurangnya berat molekul di bawah tingkat tertentu akan menyebabkan berkurangnya ketangguhan. Serat selulosa menunjukkan sejumlah sifat yang memenuhi kebutuhan pembuatan kertas.
Kesetimbangan terbaik sifat-sifat pembuatan kertas terjadi ketika kebanyakan lignin tersisih dari serat. Ketangguhan serat terutama ditentukan oleh bahan mentah dan proses yang digunakan dalam pembuatan pulp .
Molekul selulosa seluruhnya berbentuk linier dan mempunyai kecenderungan kuat membentuk ikatan-ikatan hidrogen, baik dalam satu rantai polimer selulosa maupun antar rantai polimer yang berdampingan. Ikatan hidrogen ini menyebabkan selulosa bisa terdapat dalam ukuran besar, dan memiliki sifat kekuatan tarik yang tinggi.
Gambar. Struktur Molekul Selulosa
Selulosa merupakan unsur yang penting dalam proses pembuatan pulp . Semakin banyak selulosa yang terkandung dalam pulp , maka semakin baik kualitas pulp tersebut. Berdasarkan derajat polimerisasi (DP) , maka selulosa dapat dibedakan atas tiga jenis yaitu :
-
Selulosa α ( Alpha Cellulose ) adalah selulosa berantai panjang, tidak larut dalam larutan NaOH 17,5% atau larutan basa kuat dengan DP (derajat polimerisasi) berkisar 600-1500. Selulosa α dipakai sebagai penentu tingkat kemurnian selulosa.
-
Selulosa β ( Betha Cellulose ) adalah selulosa berantai pendek, larut dalam larutan NaOH 17,5% atau basa kuat dengan DP (derajat polimerisasi) 15- 90, dapat mengendap bila dinetralkan.
-
Selulosa ɣ ( Gamma Cellulose ) adalah selulosa berantai pendek, larut dalam larut dalam larutan NaOH 17,5% atau basa kuat dengan DP (derajat polimerisasi) kurang dari 15.
Alpha Selulosa sangat menentukan sifat ketahan kertas, semakin banyak kadar alpha selulosanya menunjukkan semakin tahan lama kertas tersebut dan memiliki sifat hidrofilik yang semakin besar pada gamma dan beta selulosa daripada alpha selulosanya (Solechudin dan Wibisono, 2002)
Sifat-sifat Selulosa
Sifat-sifat selulosa terdiri dari sifat fisika dan sifat kimia. Selulosa dengan rantai panjang mempunyai sifat fisik yang lebih kuat, lebih tahan lama terhadap degradasi yang disebabkan oleh pengaruh panas, bahan kimia maupun biologis. Sifat fisika dari selulosa yang penting adalah panjang, lebar, dan tebal molekulnya. Sifat fisik lain dari selulosa adalah (Fengel dan Wenger, 1995):
-
Dapat terdegradasi oleh hidrolisa, oksidasi, fotokimia maupun secara mekanis sehingga berat molekulnya menurun.
-
Tidak larut dalam air maupun pelarut organik, tetapi sebagian larut dalam larutan alkali
-
Dalam keadaaan kering, selulosa bersifat hidroskopis, keras dan rapuh. Bila selulosa cukup banyak mengandung air maka akan bersifat lunak. Jadi fungsiair disini sebagai pelunak.
-
Selulosa dalama kristal mempunyai kekuatan lebih baik jika dibandingkan dengan bentuk amorfnya.
Proses pembuatan pulp adalah contoh perlakuan fisik dan kimia yang mempunyai tujuan untuk memisahkan selulosa dari impuritiesnya. Pemisahan dilakukan pada kondisi yang optimum untuk mencegah terjadinya degradasi terhadap selulosa. Kesulitan yang dihadapi dalam proses pemisahan ini disebabkan oleh (Fengel dan Wenger, 1995):
- Berat molekul tinggi
- Kesamaan sifat antara komponen impuritis dengan selulosa itu sendiri
- Kristalinitas yang tinggi
- Ikatan fisika dan kimia yang kuat.
Degradasi pada selulosa kadang-kadang terjadi selama proses pembuatan pulp. Keadaan ini disebabkan oleh beberapa hal, yaitu:
-
Degradasi oleh hidrolisis asam
Terjadi pada temperatur yang cukup tinggi dan berada pada media asam dalam waktu yang cukup lama. Akibat dari degradasi ini terjadi terjadinya reaksi yaitu selulosa terhidrolisa menjadi selulosa dengan berat molekul yang rendah. Keaktifan asam pekat untuk mengdegradasi selulosa berbeda-beda (Solechudin dan Wibisono, 2002).
Asam nitrat, asam sulfat dan asam chlorin adalah asam yang aktif, sedangkan asam-asam organik merupaakan asam-asam yang tidak aktif…
-
Degradasi oleh oksidator
Senyawa oksidator sangat mudah mendegradasi selulosa menjadi molekul-molekul yang lebih kecil yang disebut oxyselulosa. Hal ini terjadi tergantung dari oksidator dan kondisinya. Macam-macam oksidator adalah sebagai berikut:
-
NO3 mengoksidasi hidroksil primer dari selulosa menjadi karboksil. Oksidasi ini tidak akan memecah rantai selulosa kecuali jika terdapat alkali.
-
Chlorin mengoksidasi gugus karboksil dan aldehid. Oksidasi karboksil menjadi CO2 dan H2O, sedangkan oksidasi aldehid menjadi karboksil dan bila oksidasi diteruskan akan menjadi CO2 dan H2O.
-
Hipoklorit akan menghasilkan oksidasi selulosa yang mengandung presentase gugus hidroksil tinggi pada kondisi netral atau alkali.
-
Degradasi oleh panas
Pengaruh panas lebih besar bila dibandingkan dengan asam atau oksidator. Serat-serat selulosa yang dikeringkan pada temperatur tinggi akan mengakibatkan kertas kehilangan sebagian higroskopisitasnya (swealling ability). Hal ini disebabkan karena:
Pemanasan serat-serat pulp pada temperatur kurang lebih atau mendekati 100oC akan menghilangkan kemampuan menggembung sekitar 50% dan pemanasan diatas 200oC dan dalam waktu lama akan mengakibatkan serat- serat selulosa kehilangan strukturnya secara total.